固体・液体・気体の法則と熱
ボイルさんとシャルルさんの法則、そしてそれらを合わせた法則などがありますが、そんなものは四角四面に暗記しなくても大丈夫です。
覚えるべき公式はボイルの法則の公式1つ。
あとは、内容を覚えてください。どれがボイルの法則でどれがシャルルの法則とかはどうでもいいです。ボイル・シャルルの法則なんて、本当にどうでもいいです。
これらの公式を使用して、計算させられることもありませんので、安心してください。
気体
蒸気比重に関しては前述のページで学習したと思います。もう少し詳しく説明します。
気体や蒸気の比重は常温常圧(20℃、1気圧)ではなく、0℃、1気圧における空気1㍑の重さ(約1.293g)との比で表します。
空気の組成は、窒素約78%、酸素約20.9%の他に希ガス(He,Ne,Ar)、二酸化炭素、水蒸気等です。
これら1㍑の重さ(約1.293g)との比です。
気体の性質
ボイルの法則
温度を一定に保った状態では、一定の質量の気体の体積は圧力に反比例します。
意味分かりますか?
簡単に言うと、温度が変わらない場合、圧力をかけて圧縮すると体積が小さくなるということです。
当たり前の事です。これをグラフにすると次のようになります。P:圧力、V:体積
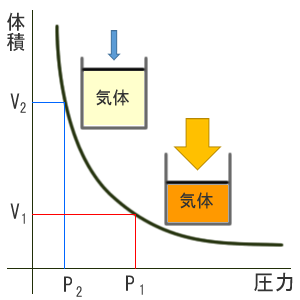
この関係を式にします。
P1×V1=P2×V2
一応覚えておいてください。過去に出題されたことがあるようです。
今度は圧力を一定にした状態の性質です。
シャルルの法則
圧力が一定なら、一定質量の気体の体積は、温度が1℃上昇または下降する毎に、0℃における体積の1/273ずつ膨張又は収縮します。
したがって、-273℃(正確には-273.15℃)以下は気体の体積が0となるため、それ以下の気温は存在しないことになります。
逆に、気温が上がって273℃になると、0℃の場合の体積の2倍になります。
ボイルシャルルの法則
質量を一定とする条件では、気体の体積は圧力に反比例し、温度に比例します。
なんだかもうわからなくなったでしょ?
温度が上がった場合に、体積が小さくなるか、圧力が高くなるかどちらかになると言っているのです。ここは、ほとんど試験に出題されません。
液体
液体も温度が上昇すれば膨張し、下降すれば収縮します。圧力による変化もありますが、これは通常の圧力では変化が起こりませんので無視してください。
液体の温度上昇に伴う体積変化は、体膨張と言います。
液体は、物質ごとに体膨張率に違いがあり、危険物取扱者試験ではガソリンや灯油などの体積を求める問題が出題されます。
ただし、毎回ではありません。
ここでは次の式が簡単なので、これだけ覚えておきましょう。
増減量=膨張率×体積×温度差
これは偶にガソリンなどの乙4危険物の膨張を問われる問題で必要となります。
固体
出題されないので割愛します。

熱
比熱・熱容量
比熱とはある物質1gの温度を1℃または1K(ケルビン)上昇させるために必要な熱量のことです。
熱の大きさを熱量といい、ジュール〔J〕または、カロリー〔cal〕の単位を用いて表示します。
水1gを1℃上昇させるために必要な熱量は1calで、1cal=4.195Jです。
この計算問題は、液体の膨張より出題率が低いです。
熱量=比熱×質量×温度差
とりあえず、全部掛け合わせると熱量が計算できます。
熱の移動
力を入れてほしいのはこの項目です。
非常に高い出題率の項目です。
熱は高温部から低温部へ伝わりますが、この伝わり方には種類があります。
伝導
熱が物質を伝ってゆく現象です。
例としては以下のような場合です。
- 鉄棒の先端を熱したら、手元の方まで熱くなってきた。
対流
液体や気体の温度差によって、液体や気体が移動する現象です。
例としては以下のような場合です。
- 風呂の湯を混ぜずにはいったら、底のほうが冷たかった。
- 部屋でストーブを使用したら、部屋の上の方だけ先に暖かくなった。
放射
熱せられた物体が放射熱を出して、他の物体に熱を与える現象です。接していなくても熱が伝わります。
例としては以下のような場合です。
- 木炭でバーベキューをしたら、顔が熱くなった。
- ストーブから離れていたのに、ストーブに向けていた背中だけが熱くなった。
- 窓ガラス越しに日光を浴びていたら暖かくなった。